Congelé à -196 °C, ce tissu cérébral de souris s’est remis à fonctionner après décongélation
Un fragment de cerveau de souris plongé dans l’azote liquide à -196 °C, puis réchauffé… et dont les neurones se remettent à communiquer entre eux comme si de rien n’était. C’est l’expérience que vient de publier une équipe allemande dans une revue scientifique de référence. Personne n’avait jamais réussi à aller aussi loin. Et les implications dépassent largement le cas de la souris.
Le pari fou d’une université allemande

L’idée de congeler un organisme vivant pour le « réveiller » plus tard alimente la science-fiction depuis des décennies. Quelques entreprises aux États-Unis et en Russie vendent déjà cette promesse à des clients fortunés : conserver un corps entier ou une tête dans l’azote liquide, en espérant qu’un jour, la technologie permette de les ramener à la vie. C’est ce qu’on appelle la cryonie. Sauf que jusqu’ici, les laboratoires n’avaient jamais réussi à prouver que des cellules cérébrales pouvaient fonctionner après un tel traitement.

C’est précisément ce que des chercheurs de l’Université Friedrich-Alexander d’Erlangen-Nuremberg viennent de démontrer. Leur étude, publiée dans la revue Proceedings of the National Academy of Sciences (PNAS), décrit comment de fines tranches d’hippocampe de souris ont survécu à une congélation à -196 °C — la température de l’azote liquide — puis ont retrouvé une activité électrique après réchauffement. Le résultat a été qualifié de « preuve de concept » par l’équipe elle-même, mais il ouvre un champ de recherche que beaucoup pensaient inaccessible.
Certains futurologues célèbres avaient prédit que ce type d’avancée arriverait, sans jamais pouvoir dire quand. Le « quand », visiblement, c’est maintenant. Mais la technique utilisée n’a rien d’un simple coup de congélateur.
Pourquoi la glace est l’ennemie n°1 du cerveau
Congeler un tissu biologique, en apparence, ça paraît simple. En réalité, c’est un cauchemar biochimique. Quand l’eau gèle, elle forme des cristaux de glace aux arêtes tranchantes. Dans un tissu aussi délicat que le cerveau, ces cristaux perforent les membranes cellulaires, déchirent les connexions entre neurones et détruisent l’architecture même du réseau neuronal. Résultat : après décongélation, il ne reste qu’une bouillie de cellules mortes.
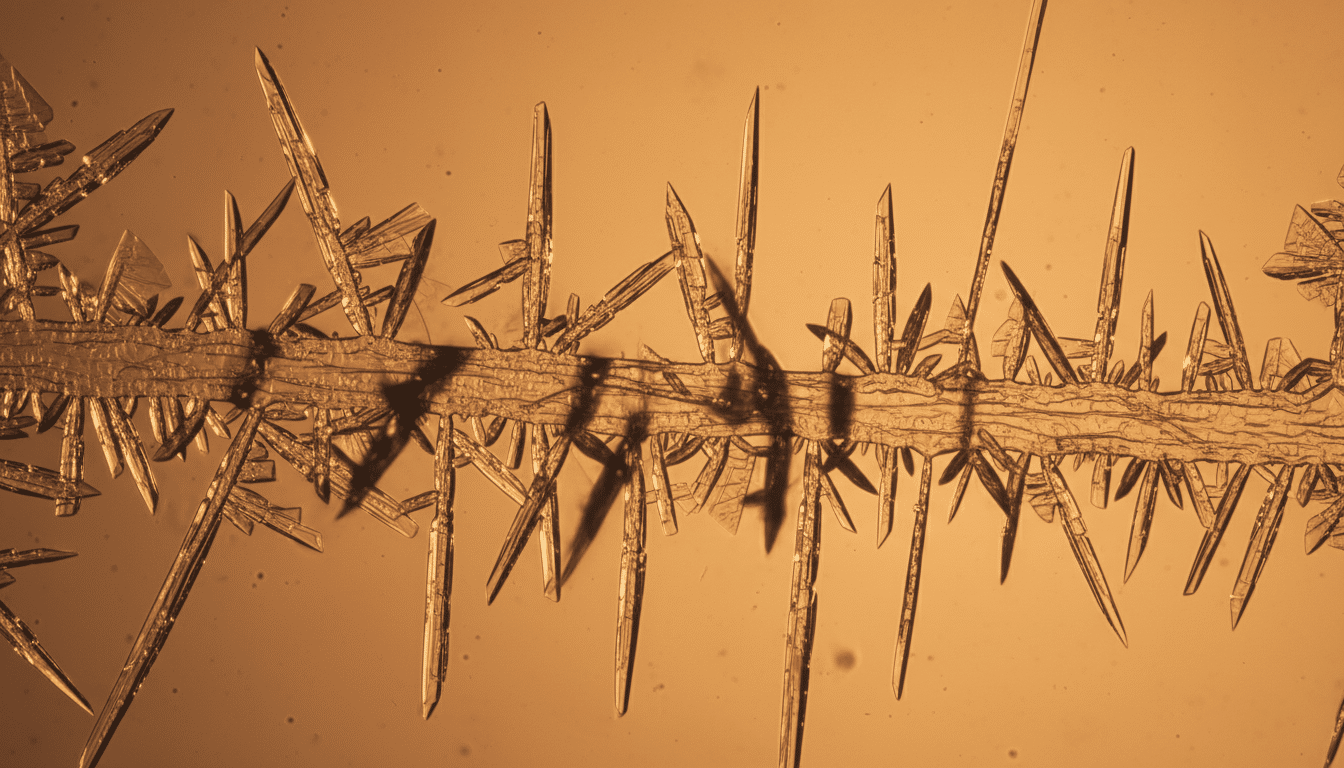
Pour contourner ce problème, les chercheurs allemands ont utilisé une technique appelée vitrification. Le principe : remplacer une partie de l’eau du tissu par un cocktail de substances cryoprotectrices avant la congélation. Ces molécules empêchent l’eau de cristalliser. Au lieu de former de la glace, elle passe dans un état dit « amorphe » — un solide désordonné, un peu comme du verre. D’où le terme vitrification.
« Nous avons optimisé la composition des conservateurs et le procédé de refroidissement afin que le tissu nerveux reste intact », explique Alexander German, l’un des auteurs de l’étude. Le dosage du cocktail protecteur et la vitesse de descente en température ont été calibrés au millimètre. Trop de cryoprotecteur, et la toxicité chimique tue les cellules. Pas assez, et les cristaux de glace font leur œuvre destructrice. Ce qui rend l’exploit d’autant plus remarquable, c’est la région choisie pour le test.
L’hippocampe : le disque dur de la mémoire
Les chercheurs n’ont pas travaillé sur n’importe quel bout de cerveau. Ils ont ciblé l’hippocampe, une structure en forme de petit hippocampe marin (d’où son nom) nichée dans les profondeurs du cerveau. C’est la zone qui gère la mémoire spatiale, l’orientation et la formation de nouveaux souvenirs. Chez les patients atteints d’Alzheimer, c’est l’une des premières régions touchées.
Les tranches d’hippocampe utilisées mesuraient quelques centaines de micromètres d’épaisseur — plus fin qu’une feuille de papier. Après immersion dans l’azote liquide et réchauffement contrôlé, les neurones de ces tranches ont recommencé à émettre des signaux électriques. Mais le plus spectaculaire est ailleurs.
L’équipe a observé un phénomène appelé potentialisation à long terme (PLT). En neurosciences, la PLT est le mécanisme fondamental de l’apprentissage : quand deux neurones communiquent de façon répétée, leur connexion se renforce. C’est le socle biologique de la plasticité cérébrale. Le fait que ce mécanisme fonctionne encore après congélation à -196 °C signifie que les circuits neuronaux n’ont pas seulement survécu — ils ont conservé leur capacité à s’adapter.
« Après décongélation, des signaux électriques se sont reformés spontanément dans l’hippocampe et se sont propagés normalement à travers les réseaux neuronaux », précisent les chercheurs. Une phrase qui, dans le monde feutré des publications scientifiques, équivaut à un cri de victoire. Mais il faut garder la tête froide — si l’on ose dire.
À lire aussi
Ce que cette expérience ne prouve pas (et c’est important)
Avant d’imaginer qu’on pourra un jour congeler un être humain et le réveiller dans 200 ans, il faut mesurer l’écart entre cette expérience et la promesse de la cryonie commerciale. Les chercheurs eux-mêmes insistent sur les limites. D’abord, il s’agit de fragments de tissu, pas d’un organe entier. Ensuite, la durée de vie de ces tissus après réchauffement reste limitée. Tous les essais n’ont pas donné les mêmes résultats.
Surtout, rien ne prouve qu’une mémoire personnelle, une identité ou une conscience puissent être préservées puis restaurées à partir d’un tel tissu. Le fait que des neurones envoient des signaux ne signifie pas que les souvenirs d’une vie sont intacts quelque part dans le réseau. La question de la survie de la conscience après la mort reste un territoire philosophique autant que scientifique.
Entre un fragment d’hippocampe de quelques centaines de micromètres et un cerveau humain de 1,4 kg irrigué par 600 km de vaisseaux sanguins, le défi est colossal. Il faudrait réussir à diffuser les cryoprotecteurs de façon homogène dans un volume incomparablement plus gros, sans toxicité, et contrôler les vitesses de refroidissement et de réchauffement avec une précision actuellement hors de portée. Les entreprises de cryonie qui conservent des corps ou des têtes dans l’azote liquide restent, pour l’instant, totalement déconnectées de ce que montre cette étude.
Même les milliardaires obsédés par l’immortalité devront attendre. Mais les applications concrètes, elles, pourraient arriver bien plus vite qu’on ne le pense.
La vraie révolution : des banques de greffons qui changeraient tout
L’application la plus réaliste — et la plus urgente — de cette technologie n’a rien à voir avec l’immortalité. Elle concerne les greffes d’organes. Aujourd’hui, le temps entre le prélèvement d’un organe et sa transplantation est dramatiquement court : quelques heures pour un cœur, un peu plus pour un rein. Ce délai impose une course contre la montre qui complique terriblement la compatibilité entre donneurs et receveurs.
Si la cryopréservation fonctionnelle devenait possible pour des organes entiers, on pourrait créer de véritables banques de greffons, conservés indéfiniment jusqu’à ce qu’un receveur compatible soit identifié. Le nombre de vies sauvées chaque année pourrait exploser. En France, environ 26 000 patients sont en attente de greffe et quelques centaines meurent chaque année faute d’organe disponible à temps. La capacité à repousser les limites biologiques est l’un des enjeux majeurs de la médecine du XXIe siècle.
En neurosciences, les retombées sont tout aussi prometteuses. Pouvoir conserver longtemps des tissus cérébraux humains prélevés lors d’interventions chirurgicales ouvrirait un champ d’étude immense pour l’épilepsie, les maladies neurodégénératives ou encore la compréhension fine du vieillissement cérébral. Aujourd’hui, ces tissus se dégradent très vite après prélèvement, limitant considérablement les recherches. Avec la vitrification, les laboratoires pourraient disposer d’échantillons parfaitement préservés pendant des mois, voire des années.
Et maintenant : un cerveau entier de souris ?
La prochaine étape annoncée par l’équipe d’Erlangen-Nuremberg est claire : appliquer la même stratégie à des tissus plus épais, puis à des cerveaux entiers de petits mammifères. Le passage de quelques centaines de micromètres à un organe complet de plusieurs centimètres représente un saut technologique majeur. La diffusion homogène des cryoprotecteurs dans un volume aussi dense que le cerveau — avec ses milliards de neurones interconnectés — reste un défi que personne n’a encore résolu.
Les innovations récentes en robotique cérébrale miniaturisée pourraient d’ailleurs jouer un rôle dans ces futures expériences, en permettant des injections de cryoprotecteurs d’une précision inédite. Le croisement de ces technologies est l’un des scénarios les plus surveillés par la communauté scientifique.
Pour l’instant, c’est un mince fragment de cerveau de souris qui porte sur ses neurones l’espoir de milliers de patients en attente de greffe. Un fragment microscopique, mais dont les signaux électriques pourraient bien résonner longtemps dans l’histoire de la médecine. Quant à savoir si la longévité humaine y trouvera un jour son compte, la réponse appartient encore aux prochaines décennies de recherche — et aux souris qui accepteront de se prêter au jeu.
