Maladies cardiaques : cette nouvelle piste venue de l’intestin intrigue les chercheurs
Les maladies cardiovasculaires restent l’une des premières causes de décès en France. Mais au-delà du mode de vie ou de la génétique. Une autre piste attire désormais toutes les attentions : celle des bactéries intestinales.
Une équipe de chercheurs basée à Séoul vient de publier des résultats qui éclairent un peu plus le mystérieux dialogue entre l’intestin et le cœur. Sans lever toutes les zones d’ombre.
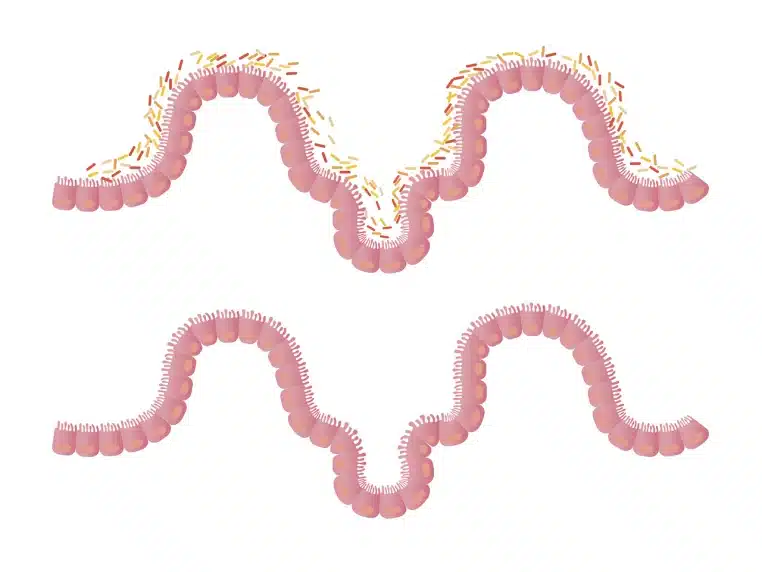
Quand l’intestin s’invite dans les maladies du cœur
Depuis plusieurs années, les spécialistes de la santé s’intéressent à l’idée que ce qui se passe dans le ventre. Ne s’arrête pas au ventre. En France, près de 140 000 personnes meurent chaque année de pathologies cardiovasculaires. Et environ 1,2 million sont hospitalisées pour ces affections. Face à un tel poids sanitaire, toute nouvelle piste de recherche devient précieuse. Même lorsqu’elle soulève presque autant de questions qu’elle n’apporte de réponses.
On sait déjà que le mode de vie, l’alimentation, le tabac ou encore la sédentarité pèsent lourd dans le risque de coronaropathie. Cette atteinte des artères du cœur qui peut conduire à l’infarctus. La génétique joue elle aussi un rôle, en rendant certaines personnes plus vulnérables que d’autres. Mais un troisième acteur se dessine peu à peu en coulisse : la communauté de micro-organismes qui peuple notre intestin.
Ces microbes intestinaux forment un véritable écosystème, parfois appelé microbiome intestinal, qui cohabite avec nous en permanence. Certains microbes sont considérés comme plutôt protecteurs. D’autres comme plus inquiétants. Mais les frontières entre les deux ne sont pas toujours aussi nettes qu’on l’imaginerait. C’est précisément ce flou que les chercheurs coréens ont tenté de clarifier.
Une étude séoulite dissèque le lien cœur–intestin
Pour explorer cette piste, l’équipe de Séoul a choisi de comparer la flore intestinale de personnes malades. Et de personnes indemnes de coronaropathie. Quatorze participants souffrant de maladie coronarienne ont fourni des échantillons de selles. Qui ont été mis en parallèle avec ceux de vingt-huit personnes non atteintes. L’objectif n’était pas seulement de dresser une liste de microbes présents. Mais de comprendre plus finement leur patrimoine génétique. Et leurs interactions possibles avec l’organisme.
Les scientifiques ont ainsi reconstitué l’ADN de chaque micro-organisme présent dans les échantillons. Cette étape permet de distinguer des espèces très proches en apparence. Mais qui n’ont pas forcément le même comportement à l’intérieur du corps. C’est un peu comme passer d’une simple photo de groupe à une véritable fiche d’identité pour chaque individu.
À partir de cette cartographie génétique. Les chercheurs ont identifié un ensemble restreint de bactéries. Particulièrement liées à la maladie coronarienne. C’est là que l’étude se distingue de nombreux travaux antérieurs. Souvent limités à des associations globales entre « dysbiose ». Et problèmes de santé, sans zoomer vraiment sur des acteurs précis.
Au fil de leurs analyses. Les auteurs ont aussi tenté de relier la présence de ces microbes à la gravité de la coronaropathie. Et pas seulement à sa simple existence. En d’autres termes, certaines signatures bactériennes semblaient aller de pair avec des formes plus sévères de la maladie. Ce qui laisse penser que l’intestin n’est peut-être pas un simple témoin passif.
Ces bactéries qui bouleversent l’équilibre de l’organisme
L’un des résultats marquants de l’étude concerne les effets observés dans le reste du corps chez les patients malades. Les chercheurs notent que certaines bactéries identifiées favorisent des modifications importantes. Notamment une inflammation accrue et des perturbations des processus métaboliques. Autrement dit, ces microbes ne se contenteraient pas d’être présents. Ils contribueraient à entretenir un terrain biologique moins favorable au cœur.
Parmi les altérations relevées figure une diminution des producteurs d’acides gras à chaîne courte. Des molécules souvent considérées comme protectrices pour la paroi intestinale. La perte de ces acteurs potentiellement bénéfiques pourrait fragiliser la barrière intestinale. Et faciliter le passage de substances pro-inflammatoires vers la circulation sanguine. Un mécanisme qui, à son tour, pourrait se répercuter sur les vaisseaux et le muscle cardiaque.
Les scientifiques mentionnent aussi une suractivation de certaines voies métaboliques. Dont le cycle de l’urée, associée à la gravité de la maladie. Ce type de dérèglement illustre à quel point l’équilibre interne peut être bousculé lorsque le microbiome se désorganise. Les bactéries ne sont donc plus de simples passagères, mais des actrices capables de modifier la chimie du corps.
Ce qui intrigue encore davantage, c’est que certaines espèces traditionnellement vues comme « gentilles » semblent pouvoir changer de visage. Dans un intestin fragilisé, elles adopteraient un comportement différent, potentiellement nocif. C’est un rappel discret qu’il n’existe pas une frontière absolue entre bonnes et mauvaises bactéries, mais plutôt un continuum dépendant du contexte général de santé.
À lire aussi

Des microbes parfois protecteurs… parfois menaçants
Cette ambivalence complique sérieusement le travail des chercheurs. Comment distinguer ce qui relève d’un microbiote réellement protecteur de ce qui n’est qu’un profil simplement différent, sans impact réel sur la maladie ? La question se pose d’autant plus que la coronaropathie résulte elle-même de multiples facteurs entremêlés, de l’alimentation à la pression artérielle en passant par le cholestérol ou le tabac.
Dans cette étude, les scientifiques constatent que la maladie pourrait transformer les microbes eux-mêmes. Autrement dit, ce n’est pas uniquement le microbiote qui influence le cœur : l’état des artères et de l’organisme en général pourrait aussi remodeler la flore intestinale. Une sorte de boucle de rétroaction, où chacun modifie l’autre.
Ce détail, que peu de gens connaissent, amène une interrogation majeure : comment savoir si une bactérie donnée favorise l’apparition de la maladie, ou si elle ne fait que refléter un organisme déjà affaibli ? Les auteurs reconnaissent qu’il reste difficile de tracer une ligne claire entre les espèces réellement pathogènes et celles dont la présence est simplement corrélée à la coronaropathie.
Certaines bactéries apparaissent comme potentiellement protectrices, d’autres comme plus liées à des formes sévères de la maladie, mais le puzzle est loin d’être complet. Les chercheurs insistent sur le fait qu’il faudra encore de nombreuses études pour démêler ces rôles, idéalement en suivant les patients sur la durée et en observant comment leur microbiote évolue avant et après la survenue de la maladie.
Un champ de recherche encore plein de zones d’ombre
Malgré ces progrès, les scientifiques restent prudents. Le champ du microbiome intestinal est encore jeune, et les études peinent souvent à passer du simple constat d’association à la démonstration d’un lien de cause à effet. Dans le cas des maladies cardiaques, cette difficulté est renforcée par la multitude de facteurs de risque déjà reconnus, de l’hypertension à la sédentarité.
Les chercheurs de Séoul rappellent qu’ils ne disposent pas encore d’une liste définitive des bactéries « amies » et des bactéries « ennemies ». La grande question non résolue consiste justement à identifier quelles souches pourraient être considérées comme réellement bénéfiques pour le cœur, et lesquelles, au contraire, aggraveraient l’état des patients.
Pour l’instant, il serait donc prématuré d’imaginer des probiotiques ciblés ou des traitements visant des espèces très précises, sur la base de cette seule étude. Mais ces travaux apportent un jalon important : ils montrent qu’il est possible de cartographier finement les interactions entre les microbes du tube digestif et la gravité de la maladie coronarienne, en allant au-delà de simples corrélations globales.
Cette approche ouvre la voie à des recherches plus ambitieuses, capables d’explorer comment l’alimentation, certains médicaments ou l’évolution d’autres pathologies viennent remodeler la flore intestinale, puis influencer en retour le système cardiovasculaire. Fin 2025, ce changement de regard sur l’intestin est déjà en soi une petite révolution.
Vers un microbiote utilisé comme outil pour protéger le cœur ?
Même si de nombreuses inconnues demeurent, l’étude sud-coréenne renforce une intuition de plus en plus partagée : nos bactéries intestinales pourraient devenir, à terme, un véritable outil de prévention cardiovasculaire. En observant la composition du microbiote, les médecins espèrent un jour mieux évaluer la vulnérabilité d’un patient, voire suivre l’efficacité d’un traitement.
On peut imaginer, à long terme, des stratégies visant à rééquilibrer la flore intestinale pour limiter l’inflammation ou restaurer la production d’acides gras protecteurs. Mais pour l’instant, ces scénarios relèvent encore de la perspective, pas du quotidien des cabinets ou des hôpitaux. Les auteurs insistent d’ailleurs sur la nécessité de multiplier les cohortes et de confirmer leurs résultats dans des populations plus larges.
Ce qui ressort clairement, en revanche, c’est que l’intestin ne peut plus être considéré comme un simple spectateur dans l’histoire des maladies cardiaques. Il en devient un acteur à part entière, capable d’influencer la gravité de la coronaropathie et de se transformer lui-même au contact de la maladie.
La conclusion des chercheurs résume bien l’état actuel des connaissances : la grande énigme reste de savoir précisément quelles souches bactériennes sont protectrices et lesquelles sont pathogènes. C’est seulement en répondant à cette question que le microbiome intestinal pourra vraiment être utilisé comme un levier pour préserver son cœur, et que les 15 espèces aujourd’hui pointées du doigt trouveront pleinement leur place dans ce puzzle complexe.
