À 21 ans, ses gencives saignaient sans raison : les médecins découvre un cancer du sang rare
Tout a commencé par un saignement des gencives qui revenait sans cesse. À 21 ans, Amber Cunningham-Rogan, étudiante écossaise, pensait à une irritation passagère, voire à un problème dentaire banal. Elle voyait régulièrement son médecin, tant les signes s’accumulaient, sans vraiment coller entre eux. Analyses rassurantes, scanners normaux, rien n’expliquait sa fatigue ni ces sensations d’engourdissement qui gagnaient ses mains et ses jambes.

Peu à peu, le doute s’est installé. À force d’examens, une prise de sang réalisée en 2020 a enfin mis en évidence quelque chose d’anormal. Le nombre de globules blancs était bien trop élevé. La jeune femme a alors compris que l’histoire ne se jouait pas seulement au niveau des gencives. Elle a confié au Sun qu’elle « n’imaginait pas que cela pouvait avoir un lien avec un cancer ». C’est pourtant la piste que les médecins vont suivre.
Des saignements qui n’alertent pas toujours tout de suite
Un filet de sang au brossage, une légère gêne après le repas, un goût métallique en bouche… Dans la vraie vie, ces petites alertes passent souvent sous le radar. Chez Amber, ces épisodes revenaient et ne ressemblaient pas à ses habitudes. Rien d’impressionnant, rien de spectaculaire, mais une répétition qui finit par inquiéter. Dans l’attente d’une explication évidente, elle multiplie les consultations, tout en continuant ses études.
Le piège, c’est justement cette apparente banalité. Les gencives sont fragiles, la fatigue est fréquente chez les étudiants, et la douleur n’était pas au premier plan. L’ensemble formait un tableau trompeur. Jusqu’au jour où la biologie du sang va raconter une toute autre histoire.
Des signes diffus qui s’additionnent
À côté des saignements, d’autres symptômes se sont greffés. Amber ressent des fourmillements persistants, une lassitude qui ne la quittait plus, et des épisodes d’engourdissement dans les membres. Pourtant, les examens d’imagerie ne montrent rien d’alarmant. C’est un scénario frustrant pour les patients comme pour les soignants : des sensations bien réelles, mais une cause qui se dérobe.
Ces signaux, mis bout à bout, méritent néanmoins une lecture plus large. Lorsqu’un organisme produit trop de cellules sanguines, lorsque la coagulation ne se comporte plus tout à fait normalement, le corps le fait savoir de manière diffuse. Le message est discret, mais il existe.

La prise de sang qui change tout
En 2020, la voie s’éclaircit. La numération formule sanguine révèle une hyperleucocytose, c’est-à-dire un excès marqué de globules blancs. Cette donnée suffit à reconfigurer toute l’enquête médicale. Les médecins orientent alors Amber vers l’hématologie pour déterminer l’origine de cette prolifération.
Une biopsie de moelle vient confirmer le diagnostic. À partir de là, l’explication s’organise enfin autour d’un mécanisme connu des spécialistes des maladies du sang. La suite va consister à nommer ce mécanisme, à en mesurer l’ampleur et à le traiter de façon ciblée.
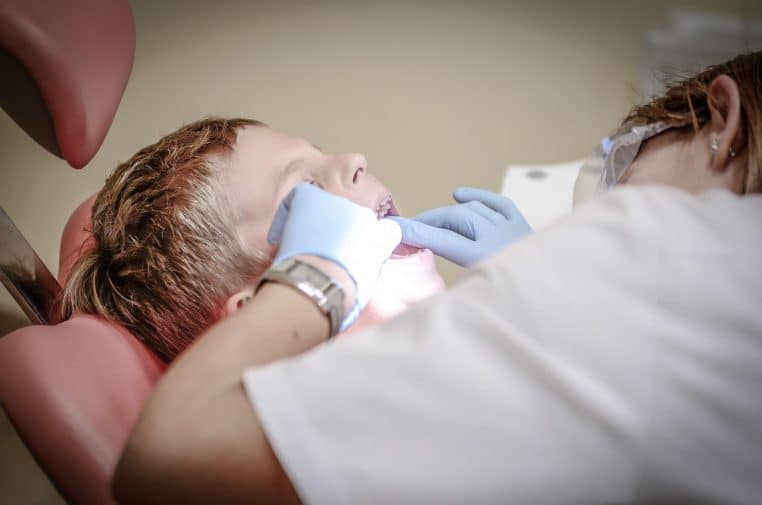
Quand la moelle osseuse s’emballe
La moelle osseuse est une véritable usine. Elle fabrique les globules rouges qui transportent l’oxygène, les globules blancs qui nous défendent contre les infections, et les plaquettes qui stoppent les saignements. Quand la chaîne s’emballe dans la mauvaise direction, elle produit trop de certaines cellules, parfois immatures, au détriment des autres.
Ce déséquilibre n’est pas qu’un chiffre sur un bilan. Il se traduit dans la vie de tous les jours par de la fatigue, des infections plus fréquentes, des ecchymoses qui apparaissent facilement, un essoufflement inhabituel, des sueurs nocturnes, parfois des douleurs osseuses ou une sensation de plénitude abdominale. Le corps subit l’encombrement.
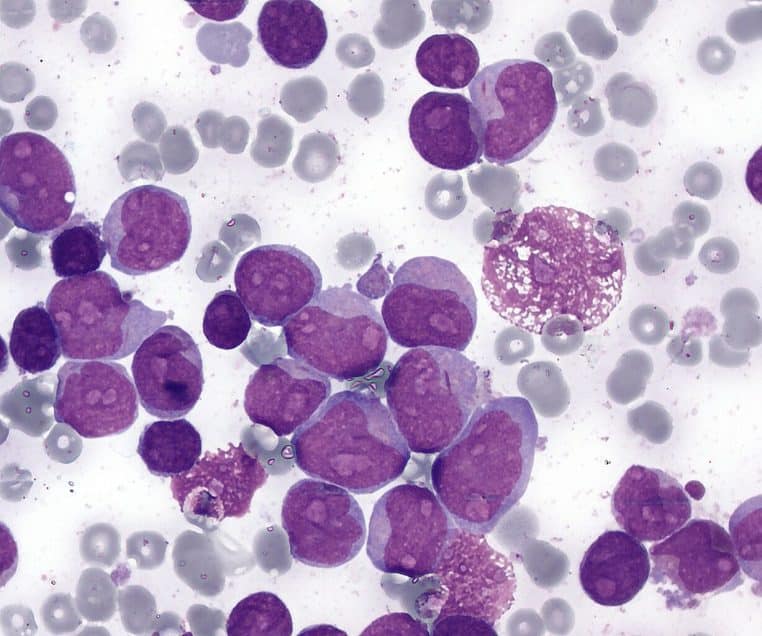
Une signature génétique bien identifiée
Dans ce tableau, un marqueur génétique occupe une place centrale : le chromosome de Philadelphie. Il résulte d’un échange de petits fragments entre les chromosomes 9 et 22. Ce « glissement » crée un gène anormal, BCR-ABL, responsable d’une protéine Bcr-Abl qui entretient la prolifération cellulaire et perturbe les mécanismes de mort programmée des cellules.
En clair, la moelle se comporte comme une chaîne de production qui ne sait plus s’arrêter. Les globules blancs se multiplient trop vite, trop longtemps, et finissent par encombrer le système. Cette signature moléculaire est aujourd’hui bien connue, au point de guider les traitements.
À lire aussi
Trois phases cliniques très différentes
Les médecins décrivent trois étapes successives possibles. La phase chronique, qui représente la grande majorité des diagnostics, correspond à une maladie encore contrôlée et relativement stable. Vient ensuite une phase accélérée, où les cellules malades gagnent du terrain. Enfin, la phase blastique marque le stade avancé, plus agressif.
Sans traitement, l’évolution peut se compter en années, parfois en mois seulement dans les formes les plus sévères. Mais l’histoire de cette maladie a radicalement changé avec l’arrivée d’une nouvelle classe de médicaments.
Des thérapies ciblées qui ont tout changé
Depuis le début des années 2000, les thérapies ciblées ont transformé la prise en charge. L’imatinib (Glivec) a ouvert la voie en bloquant l’activité de la protéine anormale issue de BCR-ABL. D’autres molécules, comme le dasatinib (Sprycel) et le nilotinib, sont venues compléter l’arsenal pour s’adapter aux différents profils de patients.
Ces traitements oraux n’effacent pas la maladie d’un claquement de doigts, mais ils la contrôlent le plus souvent sur le long terme, avec une qualité de vie sans comparaison avec l’ère d’avant. La greffe de moelle osseuse demeure la seule option véritablement curative, mais elle n’est envisagée que dans des situations bien précises, car elle reste risquée et suppose un donneur compatible.
Le parcours d’Amber : de l’inquiétude au rebond
Pour Amber, l’histoire bascule après le diagnostic. Elle commence un traitement oral ciblé et, en six mois, obtient ce que les hématologues appellent une réponse moléculaire profonde. Concrètement, le signal de la maladie devient indétectable au-delà d’un certain seuil sur les tests très sensibles. Ce n’est pas une disparition absolue, mais la preuve que le traitement a fait plier la prolifération anormale.
Cette étape ouvre parfois la porte, sous contrôle strict des médecins, à des périodes d’arrêt thérapeutique pour certaines personnes. Amber l’explique avec des mots simples : pour elle, arrêter à terme, si c’est possible et sécurisé, ce n’est pas uniquement « une question de médicaments », c’est une façon de reprendre la main sur sa vie.
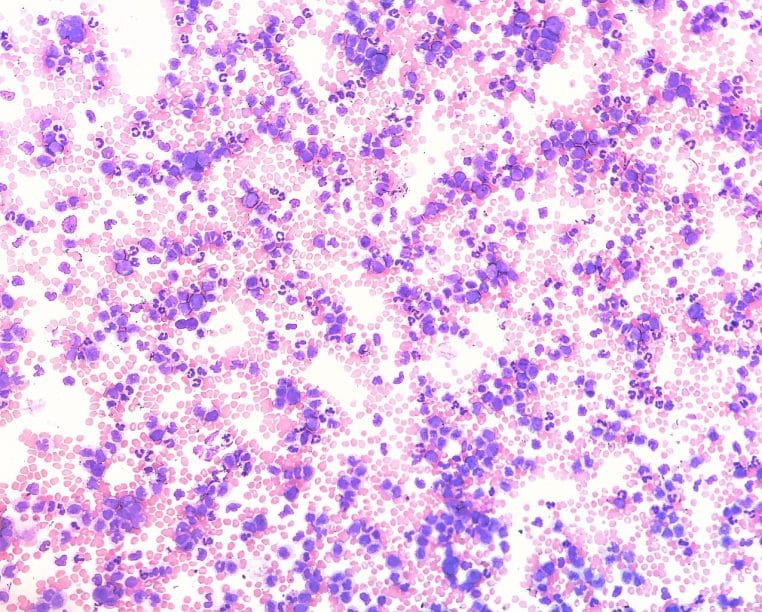
Des symptômes à ne pas balayer d’un revers de main
Faut-il pour autant s’alarmer au moindre saignement en se brossant les dents ? Non. La plupart du temps, une irritation locale, un brossage plus énergique que d’habitude ou une gingivite expliquent ces petits épisodes. Mais quand les saignements persistent, quand ils s’accompagnent d’une fatigue inhabituelle, d’ecchymoses faciles, d’infections à répétition, de fièvre ou de sueurs nocturnes, il est raisonnable de consulter et de demander une prise de sang. L’objectif n’est pas de se faire peur, mais de ne pas passer à côté d’un signal faible.
Le cas d’Amber rappelle surtout une évidence : ce n’est pas la violence d’un signe qui doit alerter, c’est sa durée, sa répétition, son association avec d’autres manifestations. C’est souvent la somme de petits indices qui finit par dessiner la bonne piste.
Aujourd’hui, une maladie rare mieux tenue en respect
Cette affection reste rare à l’échelle de la population, avec environ 600 nouveaux cas diagnostiqués chaque année en France, soit une part significative des leucémies de l’adulte. Elle touche surtout les plus de 50 ans, mais peut survenir à tout âge, comme l’illustre le parcours d’Amber. Cette diversité des profils est précisément la raison pour laquelle la surveillance et l’adaptation des traitements au cas par cas sont essentielles.
L’essentiel, c’est que les progrès thérapeutiques ont changé l’horizon. Là où l’on parlait autrefois d’une course contre la montre, on parle désormais, dans la majorité des situations, de contrôle durable de la maladie, de suivi régulier, et d’une vie qui reprend ses droits.
Le diagnostic posé à la fin de l’enquête médicale
Après des semaines de doutes, des mois d’examens, et une succession de résultats parfois contradictoires, les médecins ont enfin mis un nom sur la maladie d’Amber. Ce cancer du sang rare, lié au chromosome de Philadelphie et à l’anomalie BCR-ABL, n’explique pas seulement ses saignements des gencives : il relie aussi ses engourdissements, sa fatigue et l’excès de globules blancs détecté en 2020. Le verdict est tombé à l’issue des analyses de moelle : il s’agit d’une leucémie myéloïde chronique.
